La cataracte congénitale représente une pathologie ophtalmologique complexe dont l’évolution à l’âge adulte suscite de nombreuses interrogations. Présente dès la naissance, cette opacification du cristallin suit un parcours évolutif particulier qui diffère significativement de la cataracte acquise liée au vieillissement. L’hétérogénéité des mécanismes physiopathologiques impliqués dans les cataractes congénitales influence directement leur progression à long terme. Les patients porteurs de cette anomalie développementale nécessitent une surveillance ophtalmologique spécialisée tout au long de leur existence, car les modifications structurelles du cristallin peuvent s’accentuer avec les années. Cette évolution dépend étroitement de l’étiologie initiale, qu’elle soit génétique, métabolique ou infectieuse, et détermine les stratégies thérapeutiques à adopter.
Physiopathologie de la cataracte congénitale à l’âge adulte
Les mécanismes sous-jacents à l’évolution des cataractes congénitales reposent sur des anomalies fondamentales de l’embryogenèse cristallinienne. Ces défauts initiaux créent des zones de fragilité structurelle qui persistent tout au long de la vie. Le cristallin, dépourvu de vascularisation et d’innervation, présente une architecture particulière où les fibres cristalliniennes s’accumulent de façon concentrique depuis la formation embryonnaire. Les altérations précoces de cette organisation génèrent des contraintes mécaniques qui s’amplifient avec l’âge et les modifications physiologiques normales du cristallin.
L’accumulation progressive de protéines dénaturées dans les zones pathologiques constitue un phénomène central de l’évolution. Ces agrégats protéiques, initialement localisés aux sites d’anomalies embryonnaires, diffusent progressivement vers les régions cristalliniennes saines. Le processus de glycation non enzymatique, naturellement présent avec l’âge, s’intensifie dans ces zones fragilisées, accélérant la formation d’opacités secondaires. Cette cascade biochimique explique pourquoi certaines cataractes congénitales, initialement stables, peuvent présenter une progression notable après plusieurs décennies.
Modifications structurelles du cristallin avec le syndrome de stickler
Le syndrome de Stickler, pathologie héréditaire du tissu conjonctif, s’accompagne fréquemment de cataractes congénitales dont l’évolution présente des caractéristiques spécifiques. Les mutations affectant les gènes du collagène perturbent l’architecture capsulaire cristallinienne dès la vie fœtale. Ces anomalies capsulaires favorisent le développement d’opacités corticales qui progressent de façon centripète avec l’âge. La fragilité zonulaire associée complique la prise en charge chirurgicale et augmente le risque de complications peropératoires.
Évolution des opacités corticales dans la galactosémie héréditaire
La galactosémie héréditaire induit des cataractes congénitales caractérisées par une accumulation de galactitol dans les fibres cristalliniennes. Même après instauration d’un régime restrictif en galactose, les opacités préexistantes peuvent continuer à progresser à l’âge adulte. Le mécanisme implique une perturbation osmotique chronique des fibres cristalliniennes, créant des zones d’œdème localisé qui évoluent vers la sclérose. Cette évolution explique la nécessité d’une surveillance op
htalmologique même chez l’adulte atteint de cataracte congénitale secondaire à une galactosémie. Dans certains cas, une relative stabilité peut être observée pendant plusieurs années, puis une accélération de la dégradation cristallinienne survient à l’occasion d’un déséquilibre métabolique, d’une grossesse ou d’un épisode inflammatoire intraoculaire. On comprend ainsi pourquoi, même en l’absence de gêne visuelle majeure, il est recommandé de poursuivre un suivi régulier en consultation spécialisée, afin d’anticiper une éventuelle indication chirurgicale et d’optimiser le pronostic visuel à long terme.
Progression des cataractes zonulaires liées aux mutations PAX6
Les mutations du gène PAX6, impliqué dans la différenciation des structures oculaires, sont souvent associées à des cataractes lamellaires ou zonulaires présentes dès l’enfance. À l’âge adulte, ces opacités n’évoluent pas de manière uniforme : certaines restent limitées à une ou deux couches du cristallin, tandis que d’autres s’étendent progressivement vers le noyau ou le cortex périphérique. Cette progression résulte d’un défaut persistant de maturation des fibres cristalliniennes nouvellement formées, qui viennent se superposer aux anomalies initiales.
Sur le plan clinique, les patients présentant une cataracte zonulaire liée à PAX6 décrivent souvent une baisse de vision fluctuante, accentuée dans certaines conditions d’éclairage. Des phénomènes d’éblouissement ou de halos nocturnes apparaissent au fur et à mesure que les opacités gagnent l’axe visuel. De plus, les anomalies cornéennes et iriennes fréquemment associées aux mutations PAX6 compliquent encore la situation, en aggravant la sensibilité à la lumière et en augmentant le risque de glaucome secondaire. C’est pourquoi l’évaluation ne doit jamais se limiter au seul cristallin, mais inclure un examen complet du segment antérieur et du nerf optique.
Lorsque la cataracte congénitale zonulaire évolue, l’impact sur la réfraction est souvent marqué, avec des variations d’astigmatisme et une myopisation progressive. Pour vous, adulte concerné par ce type de cataracte, cela se traduit par des changements fréquents de correction optique et une sensation de vision « jamais parfaitement nette » malgré de nouvelles lunettes. L’ophtalmologiste doit alors peser soigneusement le rapport bénéfice/risque d’une chirurgie de cataracte, en tenant compte de la fragilité potentielle de l’iris, de la zonule et de la capsule, très fréquente dans les anomalies génétiques liées à PAX6.
Impact du vieillissement sur les fibres cristalliniennes déficientes
Avec l’avancée en âge, tout cristallin subit un processus naturel de durcissement et de jaunissement, caractéristique de la cataracte sénile. Dans le cas d’une cataracte congénitale, ces phénomènes liés au vieillissement viennent se superposer à une structure déjà altérée. Les zones de faiblesse formées dès la vie fœtale se comportent alors comme des « points d’ancrage » où s’accumulent plus rapidement les protéines oxydées et les pigments liés au stress oxydatif. Le résultat est une accentuation plus précoce des troubles visuels, parfois dès la quarantaine ou la cinquantaine.
On peut comparer le cristallin à un plancher déjà fissuré : tant que le trafic est léger, il tient bon, mais lorsque le passage augmente (ici, le vieillissement et les agressions cumulatives), les fissures se propagent. Chez l’adulte porteur d’une cataracte congénitale, les fibres cristalliniennes déficientes perdent plus vite leur capacité à maintenir une transparence homogène. Le moindre déséquilibre métabolique (diabète, tabagisme, exposition solaire chronique) agit comme un accélérateur de cette dégradation. Il n’est donc pas rare de voir une cataracte congénitale initialement modérée devenir soudainement symptomatique après un épisode général (chirurgie, maladie systémique, prise prolongée de corticoïdes).
Par ailleurs, le vieillissement modifie la plasticité du sac capsulaire et de l’appareil zonulaire. Dans un œil présentant déjà des anomalies congénitales, cela peut se traduire par des micro-déchirures capsulaires, une subluxation progressive du cristallin ou une modification de sa position, entraînant une variation brutale de la réfraction. Pour vous, cela peut se manifester par une vision qui change rapidement d’un œil à l’autre ou par une impression de « déplacement de l’image ». Ces éléments doivent alerter et conduire à un avis spécialisé, car ils modifient profondément la stratégie chirurgicale éventuelle.
Classifications morphologiques et pronostic évolutif
La classification morphologique des cataractes congénitales ne se limite pas à une description académique. Elle conditionne directement le pronostic évolutif à l’âge adulte et oriente la décision de traiter ou de surveiller. Comprendre de quel type de cataracte congénitale il s’agit permet de répondre à une question souvent posée : « Ma cataracte va-t-elle forcément s’aggraver avec le temps ? ». Certaines formes restent étonnamment stables, tandis que d’autres s’étendent insidieusement vers l’axe visuel malgré une longue période de quiescence apparente.
Cataractes polaires antérieures : progression centripète documentée
Les cataractes polaires antérieures se présentent comme de petites opacités situées sur la face antérieure du cristallin, souvent en regard de la pupille. Chez l’enfant, elles peuvent passer relativement inaperçues si leur diamètre reste inférieur à 2–3 mm. À l’âge adulte, toutefois, plusieurs études ont documenté une progression centripète lente, avec un épaississement de la lésion et une extension vers les couches sous-jacentes du cortex antérieur. Cette progression se traduit par une augmentation de la gêne à la lecture et une accentuation des halos lumineux, en particulier en lumière rasante.
Heureusement, la plupart des cataractes polaires antérieures conservent une taille limitée et ne nécessitent jamais de chirurgie. Néanmoins, dans certains contextes génétiques (antécédents familiaux de cataracte polaire opérée, anomalies capsulaires associées), l’évolution peut être plus marquée. L’ophtalmologiste surveille alors l’impact fonctionnel à l’aide de tests de sensibilité aux contrastes et de mesure précise de l’acuité visuelle. Vous pouvez ainsi constater une différence entre la vision mesurée sur l’échelle standard et la gêne ressentie au quotidien, en particulier pour la conduite nocturne.
Lorsque la lésion polaire antérieure dépasse un certain diamètre ou s’accompagne d’irrégularités capsulaires, le risque de rupture de la capsule antérieure lors de la chirurgie de cataracte augmente. Cet élément morphologique doit alors être intégré à la planification opératoire, en privilégiant des techniques de capsulorhexis assistées par des viscoélastiques de haute viscosité et, dans certains cas, par un guidage femtoseconde. Vous le voyez, une simple étiquette « polaire antérieure » recouvre en réalité des enjeux pronostiques et techniques bien distincts.
Opacifications nucléaires embryonnaires : stabilité relative chez l’adulte
Les opacifications nucléaires embryonnaires correspondent à des anomalies de la partie centrale du cristallin, formée au cours des premières semaines de la gestation. Morphologiquement, elles se présentent comme un noyau blanc ou grisâtre, souvent bien circonscrit, parfois entouré d’un anneau clair. L’une de leurs particularités majeures est leur relative stabilité au cours de la vie : de nombreuses séries cliniques montrent que ces cataractes restent quasi inchangées entre l’enfance et l’âge adulte, avec un retentissement visuel parfois modéré.
Pourquoi cette stabilité ? Le noyau embryonnaire ne se renouvelle pas : il s’agit d’un « fossile » anatomique, enfermé au cœur du cristallin, autour duquel viennent se déposer les nouvelles fibres au fil des années. Contrairement aux couches corticales périphériques, plus métaboliquement actives et vulnérables aux agressions, le noyau embryonnaire subit peu de modifications structurelles. Ainsi, chez un adulte porteur d’une opacification nucléaire congénitale, la baisse de vision est souvent liée à la survenue d’une cataracte sénile périphérique associée plutôt qu’à la progression de la lésion initiale.
Dans la pratique, cela signifie que beaucoup de patients avec une cataracte nucléaire embryonnaire peuvent être suivis de manière conservative pendant longtemps, surtout si l’acuité visuelle corrigée reste satisfaisante. En revanche, lorsque la cataracte liée à l’âge vient se surajouter, la distinction entre la lésion congénitale et l’opacification acquise perd de son importance pratique : l’indication chirurgicale repose alors avant tout sur la gêne ressentie et les besoins visuels de la personne. La connaissance de la nature embryonnaire de la cataracte reste toutefois utile pour anticiper une plus grande dureté du noyau ou une architecture capsulaire particulière.
Cataractes lamellaires zonulaires : extension périphérique progressive
Les cataractes lamellaires ou zonulaires se caractérisent par des opacités disposées en couches concentriques autour du noyau, un peu comme les cernes d’un arbre. Chez l’enfant, elles peuvent préserver une île de transparence centrale, permettant une vision relativement correcte. Avec le temps, cependant, ces anneaux opaques tendent à s’épaissir et à gagner la périphérie, ce qui perturbe la qualité optique globale du cristallin. À l’âge adulte, cette extension périphérique progressive se traduit par une altération marquée des contrastes et une gêne importante en vision mésopique.
Un point essentiel pour le pronostic est l’homogénéité des anneaux : lorsque les opacités sont irrégulières, alternant zones claires et denses, elles provoquent une diffusion lumineuse anarchique à travers le cristallin. C’est un peu comme regarder à travers un pare-brise partiellement givré : même si certaines zones restent transparentes, l’image globale est dégradée. Cette situation explique que des cataractes lamellaires modérées puissent entraîner une gêne subjective disproportionnée par rapport au degré d’opacification observé à la lampe à fente.
Sur le plan évolutif, les formes lamellaires zonulaires sont parmi les plus susceptibles de nécessiter une chirurgie de cataracte congénitale à l’âge adulte. L’extension périphérique s’accompagne souvent d’une myopisation d’indice et de variations d’astigmatisme, imposant des changements répétés de lunettes. Lorsqu’un certain seuil de désorganisation optique est franchi, la chirurgie devient le seul moyen de restaurer une qualité de vision satisfaisante, en particulier chez les patients actifs ou ceux dont la profession exige une précision visuelle fine.
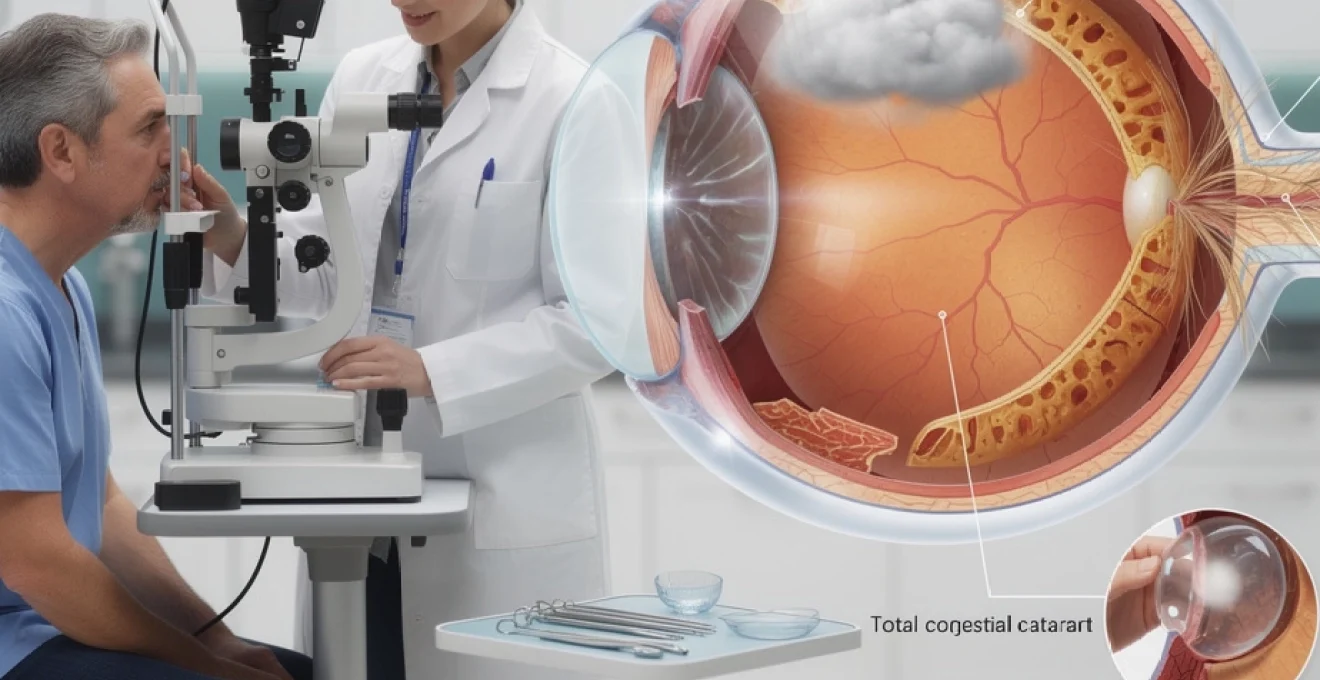
Formes totales congénitales : complications secondaires tardives
Les formes totales de cataracte congénitale, lorsqu’elles n’ont pas été opérées dans l’enfance, sont heureusement rares à l’âge adulte dans les pays disposant d’un dépistage néonatal. Lorsqu’elles persistent, elles s’accompagnent d’une amblyopie profonde et d’une faible réserve visuelle, même après extraction du cristallin. Cependant, même chez les adultes déjà opérés dans l’enfance pour une cataracte totale, des complications secondaires tardives peuvent survenir : opacification capsulaire postérieure importante, membranes rétrolenticulaires, ou encore hypertonie oculaire chronique.
Ces différents phénomènes s’expliquent par la forte activité proliférative des cellules épithéliales cristalliniennes résiduelles chez l’enfant, qui se poursuit parfois pendant des années après la chirurgie initiale. À l’âge adulte, on peut ainsi observer une fibrose capsulaire dense, des plis capsulaires majeurs ou un déplacement de l’implant intraoculaire. Ces remaniements modifient la réfraction, entraînent des aberrations optiques et peuvent nécessiter une reprise chirurgicale ou un traitement au laser YAG, parfois délicat en raison de la fragilité rétinienne associée.
Pour ces patients, le pronostic visuel dépend autant de la santé de la rétine et du nerf optique que de la transparence capsulaire. Une surveillance régulière de la pression intraoculaire, de l’épaisseur cornéenne et du champ visuel est indispensable, car le risque de glaucome secondaire augmente avec le temps. Là encore, comprendre le type initial de cataracte congénitale et l’historique chirurgical permet d’anticiper ces complications et d’adapter la prise en charge.
Surveillance ophtalmologique spécialisée des formes évolutives
À l’âge adulte, un patient porteur de cataracte congénitale – qu’elle ait été opérée ou non – ne doit jamais être considéré comme « guéri » de manière définitive. La surveillance ophtalmologique spécialisée reste la pierre angulaire de la prise en charge, car l’évolution est souvent non linéaire : longues phases de stabilité peuvent alterner avec des périodes de dégradation rapide. Une consultation tous les 12 à 24 mois est généralement recommandée, avec un rythme rapproché en cas de facteurs de risque associés (myopie forte, diabète, syndrome de Stickler, mutations PAX6).
Lors de ces consultations, plusieurs éléments sont systématiquement évalués : acuité visuelle corrigée et non corrigée, réfraction, sensibilité aux contrastes, pression intraoculaire, examen du segment antérieur à la lampe à fente et fond d’œil dilaté. Chez certains patients, un examen complémentaire par OCT maculaire ou champ visuel automatisé est utile pour dépister précocement une atteinte maculaire ou un glaucome débutant. Cette approche globale permet de distinguer la part de la cataracte congénitale dans la baisse de vision de celle imputable à d’autres pathologies associées.
Vous vous demandez peut-être : « À partir de quand doit-on envisager une chirurgie ? ». Il n’existe pas de chiffre magique d’acuité visuelle, mais plutôt un ensemble de critères : impact sur la vie quotidienne (conduite, travail sur écran, lecture), indice d’éblouissement, asymétrie entre les deux yeux et qualité de la vision binoculaire. L’ophtalmologiste tient également compte de l’état de la capsule cristallinienne, de la zonule et de la rétine, afin de planifier une éventuelle intervention dans les meilleures conditions possibles.
Enfin, la surveillance a aussi une dimension éducative : informer le patient sur les signes d’alerte (douleur oculaire, baisse brutale de vision, perception de « mouches volantes » ou de flashs lumineux) lui permet de consulter rapidement en cas de complication aiguë. Cette alliance thérapeutique est particulièrement importante chez les adultes opérés dans l’enfance qui gardent parfois un « mauvais souvenir » de leur première expérience chirurgicale et peuvent hésiter à revenir consulter. Un accompagnement clair et rassurant est donc essentiel.
Techniques chirurgicales adaptées aux anomalies cristalliniennes congénitales
La chirurgie de la cataracte congénitale chez l’adulte ne se résume pas à une simple phacoémulsification standard. Les anomalies capsulaires, zonulaires et rétiniennes fréquemment associées imposent une adaptation fine de la technique. L’évaluation préopératoire inclut une biométrie de haute précision, une topographie cornéenne et, si possible, une étude de la zonule au moyen d’un examen à la lampe à fente ou d’une imagerie de segment antérieur. L’objectif est double : sécuriser l’intervention et optimiser la puissance de l’implant intraoculaire, parfois déjà difficile à estimer chez un œil anatomiquement atypique.
Chez les patients présentant une fragilité zonulaire (syndrome de Stickler, anomalies du collagène), l’utilisation de crochets capsulaires temporaires ou d’un anneau de tension capsulaire est souvent nécessaire pour stabiliser le sac cristallinien pendant la phacoémulsification. Cette approche réduit le risque de rupture capsulaire et de luxation du noyau dans le vitré. Dans certains cas extrêmes, lorsque la zonule est très altérée, il peut être préférable de renoncer à une implantation dans le sac et d’opter pour un implant sulcus ou un implant suturé à la sclère.
Lorsque la capsule antérieure est épaissie, irrégulière ou cicatricielle – comme dans certaines cataractes polaires antérieures opérées tardivement – la réalisation du capsulorhexis peut s’avérer délicate. L’usage de colorants capsulaires (bleu trypan) et de viscoélastiques cohésifs permet de mieux visualiser et contrôler la déchirure. Dans les opacités très denses, un découpage mécanique ou assisté par laser femtoseconde peut être discuté. L’enjeu est de préserver au maximum l’intégrité capsulaire pour garantir une bonne stabilité de l’implant intraoculaire.
Enfin, le choix du type d’implant tient compte des particularités de l’œil atteint de cataracte congénitale. En présence d’amblyopie profonde ou de pathologie rétinienne associée, l’utilisation d’implants multifocaux est généralement déconseillée, car ils risquent d’aggraver les phénomènes d’éblouissement et de diminuer la qualité de vision. À l’inverse, un implant monofocal de haute qualité optique, parfois torique en cas d’astigmatisme régulier, est privilégié pour offrir la meilleure résolution possible. Chez l’adulte jeune, une légère myopie résiduelle peut être ciblée pour favoriser la vision de près sans lunettes, en fonction des besoins professionnels et des préférences du patient.
Complications spécifiques et prise en charge thérapeutique
Les adultes porteurs d’une cataracte congénitale – opérée ou non – sont exposés à un certain nombre de complications spécifiques, qui diffèrent partiellement de celles observées dans la cataracte sénile classique. Certaines sont liées à la morphologie particulière du cristallin ou de la capsule, d’autres aux anomalies associées (myopie forte, anomalies de la zonule, dystrophies rétiniennes). Les connaître permet de mieux les prévenir et de les prendre en charge rapidement, afin de préserver au maximum le capital visuel déjà fragilisé.
Glaucome secondaire par bloc pupillaire dans les cataractes intumescentes
Dans certaines formes de cataracte congénitale intumescente, le cristallin augmente de volume avec le temps, occupant une place croissante dans la chambre postérieure. Cette augmentation de volume peut entraîner un bloc pupillaire, empêchant la circulation de l’humeur aqueuse depuis la chambre postérieure vers la chambre antérieure. La pression intraoculaire s’élève alors rapidement, provoquant un glaucome aigu secondaire, parfois très douloureux. Ce scénario, bien connu dans la cataracte sénile hypermûre, peut aussi survenir dans une cataracte congénitale qui s’est modifiée avec l’âge.
Cliniquement, vous pouvez ressentir une douleur oculaire intense, une baisse brutale de la vision, des nausées et voir des halos colorés autour des lumières. Il s’agit d’une urgence ophtalmologique : un traitement médical immédiat (collyres hypotenseurs, agents osmotiques) est instauré, suivi d’une iridotomie laser ou d’une chirurgie de cataracte en urgence différée, selon la situation. La prévention repose sur le dépistage des cataractes intumescentes lors des consultations de suivi, en particulier chez les patients déjà myopes ou présentant une chambre antérieure étroite.
Décollement rétinien post-chirurgical chez les patients myopes forts
Les anomalies du développement oculaire associées aux cataractes congénitales entraînent fréquemment une myopie forte à l’âge adulte. Or, on sait que la combinaison « myopie forte + chirurgie intraoculaire » augmente le risque de décollement de rétine. Lorsqu’une chirurgie de cataracte est envisagée chez un adulte porteur de cataracte congénitale et de myopie pathologique, une vigilance accrue s’impose. Un examen minutieux de la périphérie rétinienne, avec traitement prophylactique au laser des lésions prédisposantes (trous, déchirures, palissades), est recommandé avant l’intervention.
Après la chirurgie, l’apparition soudaine de corps flottants nombreux, de flashs lumineux ou d’un voile noir dans le champ visuel doit alerter et motiver une consultation immédiate. Le décollement de rétine, lorsqu’il est pris en charge rapidement, peut être traité avec de bons résultats fonctionnels, mais tout retard réduit les chances de récupération visuelle. L’information du patient joue donc un rôle clé : savoir quels symptômes surveiller et quand consulter peut faire la différence entre une vision préservée et une séquelle irréversible.
Opacification capsulaire postérieure accélérée
L’opacification capsulaire postérieure (OCP) est la complication tardive la plus fréquente après chirurgie de cataracte, et ce d’autant plus chez les patients opérés à un âge jeune. Dans le contexte de cataracte congénitale, l’activité proliférative des cellules épithéliales cristalliniennes résiduelles est souvent plus importante, ce qui favorise une OCP précoce et parfois très dense. Chez l’adulte ayant été opéré dans l’enfance, il n’est pas rare de voir une OCP nécessitant un traitement au laser YAG dès la troisième ou quatrième décennie de vie.
Cette opacification se manifeste par une baisse progressive de la vision, une impression de voile et parfois un retour des phénomènes d’éblouissement. Le traitement par capsulotomie postérieure au laser YAG permet, dans la majorité des cas, de restaurer rapidement une transparence satisfaisante. Toutefois, chez les patients myopes forts ou présentant des anomalies rétiniennes préexistantes, ce geste n’est pas anodin : il peut légèrement augmenter le risque de décollement de rétine. Là encore, une discussion individualisée avec l’ophtalmologiste est essentielle pour peser le bénéfice attendu et le risque potentiel.
Syndrome de dispersion pigmentaire associé
Dans certains contextes anatomiques particuliers – cristallin en position antérieure, anomalies de la zonule, dysgénésies de l’iris – la cataracte congénitale à l’âge adulte peut s’accompagner d’un syndrome de dispersion pigmentaire. Le frottement mécanique entre l’iris et les structures adjacentes entraîne la libération de pigment qui se dépose sur la face postérieure de la cornée, dans le trabéculum et sur la surface de l’implant intraoculaire. À long terme, cette surcharge pigmentaire des voies d’évacuation de l’humeur aqueuse peut conduire à un glaucome pigmentaire.
Cliniquement, le patient est souvent asymptomatique au début, et seule une surveillance régulière de la pression intraoculaire et du nerf optique permet un diagnostic précoce. Des signes comme un anneau pigmenté sur la face postérieure de la cornée (anneau de Krukenberg) ou une hyperpigmentation trabéculaire à la gonioscopie orientent vers ce diagnostic. Le traitement repose sur le contrôle de la pression intraoculaire (collyres, parfois chirurgie filtrante) et, dans certains cas, sur une modification anatomique (iridotomie ou chirurgie cristallinienne) visant à réduire le frottement irido-zonulaire. Cette prise en charge précoce est particulièrement importante chez l’adulte jeune, dont l’espérance de vie visuelle est encore longue.
Pronostic visuel et facteurs prédictifs d’évolution défavorable
Le pronostic visuel d’une cataracte congénitale à l’âge adulte est extrêmement variable : certains patients conservent une vision quasi normale sans jamais être opérés, tandis que d’autres présentent une amblyopie profonde malgré des interventions multiples. Pour appréhender cette diversité, plusieurs facteurs prédictifs d’évolution défavorable ont été identifiés. Ils peuvent se regrouper en trois grandes catégories : les caractéristiques initiales de la cataracte, les conditions de prise en charge (précocité de la chirurgie, qualité de la rééducation) et les comorbidités oculaires associées.
Parmi les éléments initiaux, le caractère unilatéral de la cataracte congénitale est l’un des plus péjoratifs. La rivalité binoculaire entraîne une amblyopie de déprivation difficile à rattraper, même si la chirurgie est techniquement parfaite. De même, la densité et la localisation de l’opacité jouent un rôle majeur : une cataracte totale ou nucléaire dense prive l’œil d’une stimulation visuelle adéquate pendant la période critique du développement, réduisant la plasticité ultérieure. À l’âge adulte, ces patients présentent souvent une acuité visuelle plafonnée, malgré une transparence cristallinienne restaurée.
Les conditions de prise en charge dans l’enfance – âge de la chirurgie, respect du traitement occlusif, suivi régulier – conditionnent fortement le niveau visuel atteint plus tard. Les études montrent qu’une chirurgie tardive, après plusieurs mois ou années de privation visuelle, est associée à un pronostic nettement moins favorable. À l’inverse, une intervention précoce, couplée à une rééducation visuelle intensive, offre de meilleures chances d’obtenir une vision fonctionnelle à l’âge adulte. Cela explique pourquoi deux adultes porteurs de cataracte congénitale apparemment similaires peuvent présenter des niveaux visuels très différents.
Enfin, les comorbidités oculaires jouent un rôle déterminant : myopie forte, nystagmus, strabisme, glaucome, dystrophies rétiniennes ou anomalies du nerf optique peuvent limiter le potentiel visuel, même en l’absence d’opacité cristallinienne majeure. Chez l’adulte, l’apparition de pathologies liées à l’âge (DMLA, rétinopathie diabétique) peut également compliquer le tableau. Le pronostic ne se résume donc pas à la seule cataracte, mais doit être évalué dans une perspective globale, prenant en compte l’ensemble des structures visuelles.
Pour vous, en tant que patient ou proche, l’enjeu est de ne pas céder au fatalisme : même lorsque la vision ne peut pas être totalement restaurée, des améliorations significatives sont souvent possibles grâce à une prise en charge adaptée (chirurgie, corrections optiques, aides visuelles, rééducation). L’anticipation des facteurs de risque, la surveillance régulière et le dialogue avec l’équipe ophtalmologique permettent de choisir le bon moment et la bonne stratégie d’intervention. C’est cette approche personnalisée qui conditionne, à long terme, la qualité de vie visuelle des adultes porteurs d’une cataracte congénitale.